2014 노벨화학상 : 베칙·헬·모에너
페이지 정보
본문
"빛의 회절한계를 극복한다"
초고해상도 형광현미경 개발
 17세기에 초기 미생물학자인 안토니 판 레이우엔훅(Antonie van Leeuwenhoek)이 렌즈로 빛의 초점을 맞춰 헤엄치는 세포를 경이로운 눈으로 관찰한 이래, 현미경은 과학자들에게 새로운 발견의 가능성을 열어 줬다. 2014년 노벨 화학상은, 전통적 광학현미경의 한계에 도전하여 살아 있는 세포의 구조를 분자수준에서 고해상도로 구현한 세 명의 과학자들에게 돌아갔다. 영예의 주인공들은 미국 하워드휴즈 의학연구소의 에릭 베clr 박사, 독일 막스플랑크 생물물리 화학연구소의 스테판 헬 박사, 미국 스탠퍼드 대학교의 윌리엄 모에너 교수다.
17세기에 초기 미생물학자인 안토니 판 레이우엔훅(Antonie van Leeuwenhoek)이 렌즈로 빛의 초점을 맞춰 헤엄치는 세포를 경이로운 눈으로 관찰한 이래, 현미경은 과학자들에게 새로운 발견의 가능성을 열어 줬다. 2014년 노벨 화학상은, 전통적 광학현미경의 한계에 도전하여 살아 있는 세포의 구조를 분자수준에서 고해상도로 구현한 세 명의 과학자들에게 돌아갔다. 영예의 주인공들은 미국 하워드휴즈 의학연구소의 에릭 베clr 박사, 독일 막스플랑크 생물물리 화학연구소의 스테판 헬 박사, 미국 스탠퍼드 대학교의 윌리엄 모에너 교수다.
2014년 10월 8일 스웨덴 노벨상 위원회는 올해의 노벨화학상 수상자로 ‘초고해상도 형광현미경(Superresolution fluorescence microscopy, SRFM)’ 기술을 개발한 미국 하워드휴즈의학연구소의 에릭 베칙(Eric Betzig) 박사와 윌리엄 모너(William E. Moerner) 스탠포드대 교수, 독일 막스플랑크 생물물리화학연구소의 슈테판 헬(Stefan W. Hell) 박사를 공동으로 선정하였다.
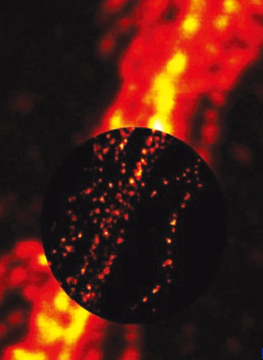 이 기술은 형광분자 표지에 의한 단일분자 검출기술과 데이터 처리 기법인 ‘점상강도 분포함수(Point-spread function, PSF)’의 알고리즘 등을 기반으로 하여 일반적인 광학현미경으로는 지금까지 관찰이 어려웠던 세포 안의 나노크기 이미지(~20 nm 공간 분해능)를 직접 관찰할 수 있는 것으로 빛의 회절한계 해상도(Diffraction limited resolution)를 극복한 획기적인 기술로 평가되고 있다.(그림 1)
이 기술은 형광분자 표지에 의한 단일분자 검출기술과 데이터 처리 기법인 ‘점상강도 분포함수(Point-spread function, PSF)’의 알고리즘 등을 기반으로 하여 일반적인 광학현미경으로는 지금까지 관찰이 어려웠던 세포 안의 나노크기 이미지(~20 nm 공간 분해능)를 직접 관찰할 수 있는 것으로 빛의 회절한계 해상도(Diffraction limited resolution)를 극복한 획기적인 기술로 평가되고 있다.(그림 1)
세포의 내부세계를 드러낸 세 명의 과학자들
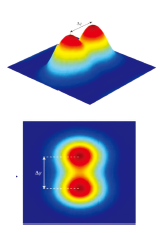 3인 공동연구자의 업적을 좀 자세히 살펴보면 다음과 같다. 독일의 언스트 아베 (Ernst Abbe)에 의하면 일반적으로 빛의 회절한계에 의해 이웃한 두 물질의 공간 분해능(spatial resolution) Rx,y = λ/2NA (여기서 λ는 형광을 일으키기 위해 사용되는 들뜸 빛의 파장, NA는 현미경 대물렌즈의 개구수)에 의해 회절한계 분해능은 ~200 nm로 알려져 왔다(그림 2).
3인 공동연구자의 업적을 좀 자세히 살펴보면 다음과 같다. 독일의 언스트 아베 (Ernst Abbe)에 의하면 일반적으로 빛의 회절한계에 의해 이웃한 두 물질의 공간 분해능(spatial resolution) Rx,y = λ/2NA (여기서 λ는 형광을 일으키기 위해 사용되는 들뜸 빛의 파장, NA는 현미경 대물렌즈의 개구수)에 의해 회절한계 분해능은 ~200 nm로 알려져 왔다(그림 2).
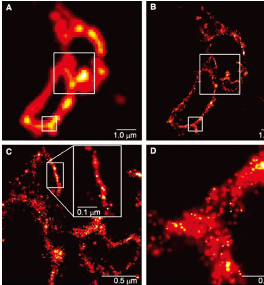 하지만, 에릭 베칙 등은 2006년 25 – 100 nm 나노미터의 분리도로 세포 내 단백질의 광학이미지를 얻는 방법을 발표하였다. 광활성 형광단백질 분자들의 수많은 작은 부분들을 활성화시키고, 국지화 한 다음, 다시 빛에 의해 그것을 사라지게 하였다. 그들은 ‘광활성된 국지화 현미경(Photoactivated localization microscopy, PALM)’이라고 하는 현미경 기술을 개발하여 리소좀과 미토콘드리아의 얇은 막 안의 특정 단백질의 정확한 위치와, 고정된 전세포(whole cell)에서 초점접착역(focal adhesions)에서의 빈쿨린 (vinculin)과 접착용 세포족(lamellipodium) 안의 액틴(actin) 이미지, 원형질 막에서RNA 종양 바이러스의 단백질 Gag 분포도를 영상화 할 수 있었다(그림 3). 이들은 PALM을 사용하여 COS-7 세포에서 전반사형광현미경(TIRFM)을 이용하여 측정 할 수 없었던 리소좀(lysosome) 혹은 엔도솜(endosome)들이 상호작용과 리소좀막 안의 CD63 단백질 분포를 10 nm 크기 수준에서 정확히 측정 할 수 있었다.
하지만, 에릭 베칙 등은 2006년 25 – 100 nm 나노미터의 분리도로 세포 내 단백질의 광학이미지를 얻는 방법을 발표하였다. 광활성 형광단백질 분자들의 수많은 작은 부분들을 활성화시키고, 국지화 한 다음, 다시 빛에 의해 그것을 사라지게 하였다. 그들은 ‘광활성된 국지화 현미경(Photoactivated localization microscopy, PALM)’이라고 하는 현미경 기술을 개발하여 리소좀과 미토콘드리아의 얇은 막 안의 특정 단백질의 정확한 위치와, 고정된 전세포(whole cell)에서 초점접착역(focal adhesions)에서의 빈쿨린 (vinculin)과 접착용 세포족(lamellipodium) 안의 액틴(actin) 이미지, 원형질 막에서RNA 종양 바이러스의 단백질 Gag 분포도를 영상화 할 수 있었다(그림 3). 이들은 PALM을 사용하여 COS-7 세포에서 전반사형광현미경(TIRFM)을 이용하여 측정 할 수 없었던 리소좀(lysosome) 혹은 엔도솜(endosome)들이 상호작용과 리소좀막 안의 CD63 단백질 분포를 10 nm 크기 수준에서 정확히 측정 할 수 있었다.
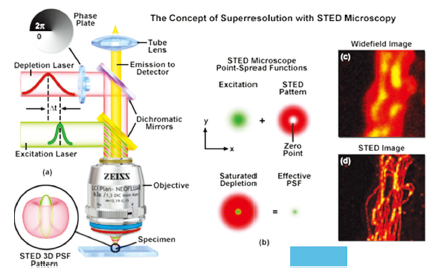
 스테판 헬 등은 ‘원거리장 형광현미경(Far-field fluorescence microscopy)’에서 한정된 초점크기와 분해 한계의 원인이 되는 회절장벽을 기본적으로 무너뜨렸다. STED 초고해상 현미경은 유도방출을 통한 초점의 테두리에서 들뜬 유기분자를 소광시켜 이미지를 얻을 수 있었다(그림 4). 광학 축에 따라 점의 크기가 분해한계의 6배까지 축소할 수 있었으며 90–110 nm 직경을 갖는 새로운 구 모양의 형광 점을 만들었다. 이것을 이용하여 살아있는 세포의 이미지를 더 정교하게 나타낼 수 있었다(PNAS, 97, 8206–8210, 2000). 일반적으로 STED에서 도넛-모양의 고갈레이저 장은 굴절한계 이상의 분해능을 증가시키기 위해서 들뜸 레이저의 ‘점상강도 분포함수(PSF)’를 효율적으로 좁게 만들 수 있으며, 측면치수에서 최상의 경우 약 20 nm까지 접근할 수 있었다.
스테판 헬 등은 ‘원거리장 형광현미경(Far-field fluorescence microscopy)’에서 한정된 초점크기와 분해 한계의 원인이 되는 회절장벽을 기본적으로 무너뜨렸다. STED 초고해상 현미경은 유도방출을 통한 초점의 테두리에서 들뜬 유기분자를 소광시켜 이미지를 얻을 수 있었다(그림 4). 광학 축에 따라 점의 크기가 분해한계의 6배까지 축소할 수 있었으며 90–110 nm 직경을 갖는 새로운 구 모양의 형광 점을 만들었다. 이것을 이용하여 살아있는 세포의 이미지를 더 정교하게 나타낼 수 있었다(PNAS, 97, 8206–8210, 2000). 일반적으로 STED에서 도넛-모양의 고갈레이저 장은 굴절한계 이상의 분해능을 증가시키기 위해서 들뜸 레이저의 ‘점상강도 분포함수(PSF)’를 효율적으로 좁게 만들 수 있으며, 측면치수에서 최상의 경우 약 20 nm까지 접근할 수 있었다.
분자생물학 발전 및 질병예방에 크게 공헌
 결론적으로, 지난 수십 년 동안 형광현미경은 생체분자의 폭 넓은 다양성, 반응경로 그리고 살아있는 세포, 조직, 모든 동물 안에서 역학을 조사하기 위한 필수적인 도구가 되어왔다고 할 수 있다. 전자현미경 기술과는 다르게 형광이미지는 배양액에서 유지되고 있는 세포와 호환이 잘 되어, 장시간 동안 발생하는 현상에 대해 광학적 기반을 둔 관측을 가능하게 하였다. 공간 분리도에서 양전자방사단층촬영, 자기공명 이미징, 단층촬영장치 등을 포함하는 몇몇 기술들은 1mm와 10μm 사이의 분리도에서 동물이나 사람의 이미지를 생성할 수 있는 반면 전자현미경이나 주사식 탐침 기술은 가장 높은 공간적 분리도를 가지며 어떤 경우에는 분자나 원자 수준까지 측정이 가능하다(그림 5).
결론적으로, 지난 수십 년 동안 형광현미경은 생체분자의 폭 넓은 다양성, 반응경로 그리고 살아있는 세포, 조직, 모든 동물 안에서 역학을 조사하기 위한 필수적인 도구가 되어왔다고 할 수 있다. 전자현미경 기술과는 다르게 형광이미지는 배양액에서 유지되고 있는 세포와 호환이 잘 되어, 장시간 동안 발생하는 현상에 대해 광학적 기반을 둔 관측을 가능하게 하였다. 공간 분리도에서 양전자방사단층촬영, 자기공명 이미징, 단층촬영장치 등을 포함하는 몇몇 기술들은 1mm와 10μm 사이의 분리도에서 동물이나 사람의 이미지를 생성할 수 있는 반면 전자현미경이나 주사식 탐침 기술은 가장 높은 공간적 분리도를 가지며 어떤 경우에는 분자나 원자 수준까지 측정이 가능하다(그림 5).
분해능에서 이런 2개의 극단 예 사이에 광학현미경이 놓여있다. 즉, 살아있는 세포를 이미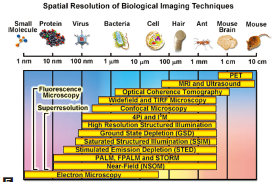 징화 할 수 있는 것에서 유도되는 장점 외에 광역(widefield), 레이저주사(laser scanning), 회전디스크(spinning disk), 다광자(multiphoton), 전반사(total internal reflection) 등을 포함하는 형광현미경 형태의 가장 큰 단점은 1800년 대 후반 아베에 의해 처음으로 설명되고 묘사된 공간분해능의 한계라 할 수 있을 것이다.
징화 할 수 있는 것에서 유도되는 장점 외에 광역(widefield), 레이저주사(laser scanning), 회전디스크(spinning disk), 다광자(multiphoton), 전반사(total internal reflection) 등을 포함하는 형광현미경 형태의 가장 큰 단점은 1800년 대 후반 아베에 의해 처음으로 설명되고 묘사된 공간분해능의 한계라 할 수 있을 것이다.
하지만, 1990년 대 후반 스페판 등에 의해 개척된 근본적으로 새로운 현미경기술은 아베의 회절한계를 극복할 수 있었으며 이것은 궁극적으로 형광현미경의 혁명을 가져오게 되었다. 결과적으로 10nm 혹은 그 이하의 공간적 분해능을 갖는 많은 방법론이 최근에 소개되고 있으며 지금은 이것들을 총괄하여 ‘초고분해능 현미경(Superresolution microscopy, SRM)’이라 부르고 있다.
SRM이미징에서 가장 중요한 발전은 원거리장현미경(far-field microscopy)으로도 측정이 가능하며, 밝고 어두운 상태 사이의 전환이 가능한 형광단(fluorophore)의 두 분자 사이에서의 전이를 공간적 혹은 시간적으로 조절 가능하다는 것이다. 또한 들뜨기 조명에서 사용되는 PSF의 크기를 물리적으로 줄일 수 있다는 것이다. 앞으로 SRM 기술 응용은 생명현상의 정확한 이해를 가능하게 할 것이며, 이로 인해 질병진단 정확성이 획기적 증진하여 원천적인 질병치료 및 예방 가능할 것으로 사료된다.
 글 | 강성호 교수(경희대학교 응용화학과)
글 | 강성호 교수(경희대학교 응용화학과)
강성호 교수는 서울대학교에서 생분석화학 박사학위를 취득한 후, 미국 에임스 국립 연구소 에너지 부(Ames Lab-US Department of Energy)에서 ‘휴먼게놈프로젝트(HGP)’의 연구원으로 근무하다 2000년 삼성종합기술원 책임연구원으로 귀국했다. 2010년 9월부터는 경희대학교 응용화학과에서 재직 중이다. 대한화학회 분석화학분과 감사/운영위원과 한국바이오칩학회 이사를 맡고 있으며, 주 관심 분야는 차세대 나노바이오 센서, 바이오칩 개발, 새로운 초분해능 광학현미경 기술 개발이다.
